Kontaktní osoba: Bohumír Grüner
Vědci z Oddělení syntéz ÚACh hrají klíčovou roli v širší multioborové spolupráci zaměřené na vývoj biologicky aktivních karboranů a metallakarboranů, na níž se podílí návrhem a syntézou nekonvenčních biologicky aktivních látek. Biologické studie probíhají v rámci spolupráce týmy s ÚMG AV ČR, ÚOChB AV ČR, BFÚ AV ČR Brno, ÚMCh AV ČR, Ústavem Molekulární a Translační Medicíny při Universitě Palackého University v Olomouci (ÚMTM) a IKEM Praha.
Návrh a syntéza farmakologicky relevantních klastrových sloučenin boru
Nadějné výsledky ve vývoji specifických inhibitorů enzymu karbonická anhydráza IX (CA-IX)1 poskytly inspiraci pro pokračování výzkumu v oblasti s ohledem na použití látek v zobrazovacích metodách a hledání dalších vhodných farmakologických cílů pro chemickou intervenci pomocí borových klastrů. Přítomnost enzymu CA-IX je vázána na povrch buněk hypoxických nádorů a patří v současné době k validovaným cílům pro léčbu onkologických onemocnění a jejich diagnostiku.
Řada nově vyvinutých chemických postupů umožnila syntézu substitučních derivátů karboranů and kobalt bis(dikarbollid)ového iontu s koncovou sulfonamidovou (či podobnou) skupinou [2-4], u níž je známo, že je schopna poskytovat silnou vazbu s atomem Zn2+ v aktivním místě CA-IX. Tyto nové anorganické inhibitory CA-IX jsou aktuálně dostupné ve třech až šesti reakčních krocích a vykazují nadějnou in vitro aktivitu s Ki hodnotami v intervalu od nízkých nanomolárních až po pikomolární (20 pM pro dosud nejúčinnější inhibitor). Nejlepší hodnoty selektivitního faktoru CAIX/ CAII dosahují aktuálně 668 (pro metallakarboran) a 1312 (pro karboran) [5]. Souběžně prováděné strukturní, fyzikálně-chemické a teoretické studie komplexů enzym-inhibitor, které jsou prováděny ve spolupráci s IOCB CAS a ÚMG CAS (Obr. 1 a 2), poskytly dobré vodítko pro pochopení SAR [6-8].
Další studium farmakologicky relevantních faktorů jako např.: in vitro cytotoxických vlastností, vazby na sérové proteiny, průniku přes buněčné membrány a in vivo toxikologických, farmakokinetických a aktivitních studií na myším xenotransplantátu, prováděné ve spolupráci s ÚMTM, potvrdily nadějné vlastnosti sloučenin [5]. Tyto inhibitory mohou být tudíž považovány za vhodné kandidáty pro další vývoj lékových formulací využitelných v léčbě onkologických onemocnění. Navíc byla u iontových sloučenin prokázány možnost jejich využití pro účinný transport cytostatik jako Doxorubicin přes buněčnou membránu.
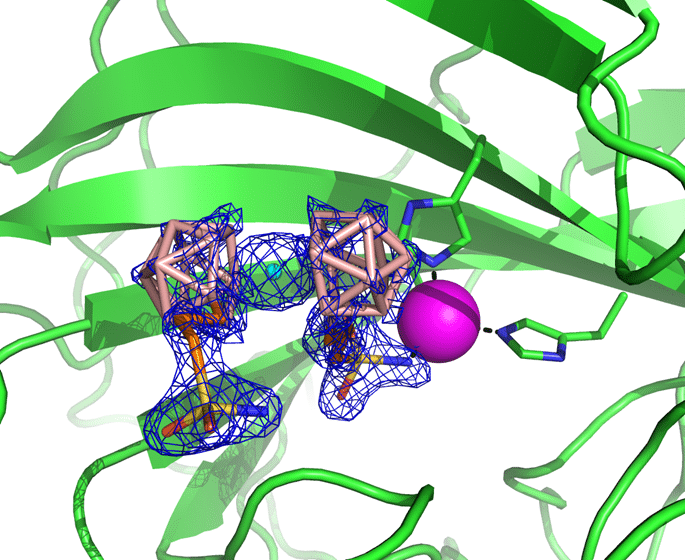
Obr. 1: Struktura metallacarboranového inhibitoru CB-31 v aktivním místě CA-29 (CA-IX mimic) enzymu. Stanovení struktury: J. Brynda, P. Řezáčová, ÚMG AV ČR, ÚOChB, AV ČR.
![Obr. 2: Překryv struktury metallakarboranového inhibitoru CB-30 v aktivním místě enzymu CA-29 (CA-IX mimic) se strukturně nejjednodušším inhibitorem na základě ortho-karboranu [1], obě látky nesou po jedné alkylsulfamidové skupině. Struktury poskytují vodítko pro vysvětlení pozorované vyšší aktivity v případě využití metallakarboranů, a to v důsledku jejích lepších interakcí s oběma kapsami enzymu a mnohonásobným sterickým kontaktům v okolí aktivního centra. Stanovení struktury: J. Brynda, P. Řezáčová, ÚMG AV ČR, ÚOChB, AV ČR.](https://www.iic.cas.cz/wp-content/uploads/2025/01/Med-Fig-2.png)
Obr. 2: Překryv struktury metallakarboranového inhibitoru CB-30 v aktivním místě enzymu CA-29 (CA-IX mimic) se strukturně nejjednodušším inhibitorem na základě ortho-karboranu [1], obě látky nesou po jedné alkylsulfamidové skupině. Struktury poskytují vodítko pro vysvětlení pozorované vyšší aktivity v případě využití metallakarboranů, a to v důsledku jejích lepších interakcí s oběma kapsami enzymu a mnohonásobným sterickým kontaktům v okolí aktivního centra. Stanovení struktury: J. Brynda, P. Řezáčová, ÚMG AV ČR, ÚOChB, AV ČR.
Multioborové a mezinárodní spolupráce
S ohledem na fakt, že znalosti o působení polyhedrálních látek na složky živých systémů jsou dosud značně omezené, výzkum v oblasti biologických látek probíhá současně s experimentálním, teoretickým a fyzikálně-chemickým studiem různých typů jejich interakcí s přírodními a modelovými systémy. Toto studium probíhá v rámci spolupráce ÚMTM, ÚMG, ÚOChB a BFÚ. Ve spolupráci s Constructor University v Brémách, SRN jsou studovány interakce substituovaných iontových klastrových sloučenin boru se supramolekulárními platformami, modelovými a přírodními buněčnými membránami a vybranými buněčnými liniemi. Nedávno bylo zjištěno, že objemné klastrové borátové anionty jsou schopny přenášet impermeabilní kationické proteiny přes buněčnou membránu.9, 10 Souběžně probíhá spolupráce s BFÚ CAS na pochopení redoxního chování látek ve vodném roztoku za použití elektrochemických metod a využití vybraných metallakarboranových strukturních bloků pro značení biomolekul. Aktuální cíle jsou zaměřeny na strukturní modifikace, které umožní snadnou a specifickou konjugaci s bio-makromolekulami a ladění elektrochemického okna a odezvy klastrových značek [11-13].
Publikace:
- B. Grüner, J. Brynda, V. Das, V. Šícha, J. Štěpánková, J. Nekvinda, J. Holub, K. Pospíšilová, M. Fábry, P. Pachl, V. Kral, M. Kugler, V. Mašek, M. Medvědíková, S. Matějková, A. Nová, B. Lišková, S. Gurská, P. Džubak, M. Hajdůch and P. Řezáčová, J. Med. Chem., 2019, 62, 9560-9575.
- J. Dvořanová, M. Kugler, J. Holub, V. Šícha, V. Das, J. Nekvinda, S. El Anwar, M. Havránek, K. Pospíšilová, M. Fábry, V. Král, M. Medvedíková, S. Matějková, B. Lišková, S. Gurská, P. Džubák, J. Brynda, M. Hajdůch, B. Grüner and P. Řezáčová, European Journal of Medicinal Chemistry, 2020, 200, 13.
- J. Nekvinda, M. Kugler, J. Holub, S. El Anwar, J. Brynda, K. Pospíšilová, Z. Růžicková, P. Řezáčová and B. Grüner, Chem.-Eur. J., 2020, 26, 16541-16553.
- B. Grüner, M. Kugler, S. El Anwar, J. Holub, J. Nekvinda, D. Bavol, Z. Růžicková, K. Pospíšilová, M. Fábry, V. Král, J. Brynda and P. Řezáčová, ChemPlusChem, 2021, 86, 352-363.
- M. Kugler, J. Nekvinda, J. Holub, S. El Anwar, V. Das, V. Šícha, K. Pospíšilová, M. Fábry, V. Král, J. Brynda, V. Kašička, M. Hajdůch, P. Řezáčová and B. Grűner, ChemBioChem, 2021, 22, 2741-2761.
- M. Kugler, J. Holub, J. Brynda, K. Pospíšilová, S. El Anwar, D. Bavol, M. Havránek, V. Král, M. Fábry, B. Grüner and P. Řezáčová, J. Enzym. Inhib. Med. Chem., 2020, 35, 1800-1810.
- J. Fanfrlík, J. Brynda, M. Kugler, M. Lepšik, K. Pospíšilová, J. Holub, D. Hnyk, J. Nekvinda, B. Grűner and P. Řezáčová, Phys. Chem. Chem. Phys., 2023, 25, 1728-1733.
- V. Šolínová, J. Brynda, V. Šícha, J. Holub, B. Grűner and V. Kašička, Electrophoresis, 2021, 42, 910-919.
- Y. Chen, A. Barba-Bon, B. Grüner, M. Winterhalter, M. A. Aksoyoglu, S. Pangeni, M. Ashjari, K. Brix, G. Salluce, Y. Folgar-Cameán, J. Montenegro and W. M. Nau, J. Am. Chem. Soc., 2023, 145, 13089-13098.
- G. Salluce, Y. Folgar-Cameán, A. Barba-Bon, I. Niksic-Franjic, S. El Anwar, B. Grüner, I. Lostalé-Seijo, W. M. Nau and J. Montenegro, Angew. Chem.-Int. Edit., 2024, 63, 9.
- S. El Anwar, L. Pazderová, D. Bavol, M. Bakardjiev, Z. Ružičková, O. Horáček, L. Fojt, R. Kučera and B. Grüner, Chem. Commun., 2022, 58, 2572-2575.
- L. Fojt, B. Gruner, J. Holub, L. Havran and M. Fojta, J. Electroanal. Chem., 2022, 910, 8.
- L. Fojt, J. Nekvinda, S. El Anwar, B. Grüner, L. Havran and M. Fojta, Electroanalysis, 2020, 32, 1859-1866.